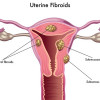
Patofisiologi Mioma Uteri
Patofisiologi mioma uteri adalah tumor monoklonal yang tumbuh dari jaringan otot halus di uterus yaitu pada lapisan miometrium. Tumor ini tergolong dalam tumor jinak yang terdiri dari miofibroblas yang tidak beraturan yang terkubur dalam matriks ekstraseluler yang berjumlah besar. Matriks ekstraseluler ini sendiri berkontribusi cukup besar pada volume tumor. Kejadian yang mencetuskan tumor ini sendiri masih belum diketahui secara pasti.[1-4]
Patogenesis
Paling tidak terdapat dua komponen yang berbeda yang berkontribusi dalam pertumbuhan mioma uteri, yaitu:
- Transformasi miosit-miosit normal menjadi miosit yang tidak normal, akibat mutasi somatik
- Pertumbuhan miosit-miosit yang tidak normal menjadi tumor yang nampak secara klinis[1-3]
Stem cells miometrium diketahui tumbuh menjadi mioma uteri di bawah pengaruh beberapa hormon. Selain itu, faktor-faktor lainnya, seperti genetik, tidak beraturannya matriks ekstraseluler, dan faktor-faktor pertumbuhan juga ditemukan memiliki peran dalam terbentuknya mioma uteri.[1-3]
Hormonal
Sel-sel pada mioma berproliferasi dengan kecepatan sedang dan pertumbuhannya tergantung dari hormon-hormon steroid yang diproduksi oleh ovarium yaitu estrogen dan progesteron. Adanya ketergantungan terhadap hormon-hormon ini yang menyebabkan menciutnya sebagian besar kasus mioma uteri setelah menopause.[1,2,4]
Estrogen estradiol yang poten akan menginduksi produksi reseptor progesteron melalui reseptor estrogen alfa (ER-α). Reseptor-reseptor progesteron ini merupakan komponen penting dalam respons jaringan mioma terhadap progesteron yang disekresi oleh ovarium.
Oleh karenanya, baik progesteron dan reseptor progesteron sangat diperlukan bagi terjadinya pertumbuhan tumor, peningkatan proliferasi sel, serta bagi ketahanan dan peningkatan pembentukan matriks-matriks ekstraseluler. Estrogen dan ER-α sendiri tidaklah cukup untuk pertumbuhan mioma uteri tanpa adanya progesteron dan reseptor progesteron. [1,2,4]
Teori hormonal ini dapat menjelaskan mengenai efek konsumsi morning-after-pill yang diperkirakan dapat mencegah risiko myoma uteri. Morning-after-pill yang mengandung oral synthetic progesterone receptor modulator (SPRM) diperkirakan dapat efek antigonis parsial terhadap progesteron sehingga mencegah proliferasi sel tumor fibroid uteri.[32]
Genetik
Meskipun dulunya mioma uteri tidak dianggap sebagai penyakit genetik, berbagai bukti-bukti klinis yang baru menunjukkan bahwa faktor genetik berperan pada paling tidak sebagian kasus mioma uteri.
Beberapa survei-survei sitogenik menunjukkan bahwa pada sekitar 40% mioma uteri mengalami perubahan kromosom dan memiliki anomali sitogenik yang sama dengan beberapa tipe tumor yang lain. Sebagai contoh yaitu di mana beberapa penelitian yang menunjukkan adanya translokasi antara kromosom 12 dan 14, trisomi 12, translokasi antara kromosom 6 dan 10, serta delesi kromosom 3 dan 7.
Gen-gen yang diduga terlibat dalam munculnya mioma uteri yang paling sering di antaranya yaitu High Mobility Group A2 (HMGA2), regulator transkripsi mediator complex subunit 12 (MED12), mutase pada collagen type IV, alpha-5 dan alpha-6 (COL4A5 dan COL4A6).[1,2,4]
Matriks Ekstraseluler
Komponen-komponen matriks ekstraseluler yang tidak beraturan juga merupakan salah satu karakteristik khas dari pertumbuhan mioma. Matriks ekstraseluler ini sebagian besar terdiri dari berbagai subtipe kolagen, fibronektin, dan proteoglikan.
Baru-baru ini beberapa subtipe kolagen ditemukan terekspresi lebih banyak pada sel-sel mioma dibandingkan pada sel-sel miometrium, seperti COL1A1, 4A2, 6A1, 7A1, dan 16A1.[1,2]
Faktor-faktor Pertumbuhan
Beberapa faktor-faktor pertumbuhan juga ditemukan berperan dalam terbentuknya mioma uteri. Faktor-faktor ini di antaranya yaitu vascular endothelial growth factor (VEGF), epidermal growth factor (EGF), heparin binding epidermal growth factor (HB-EGF), protein derived growth factor (PDGF), insulin-like growth factor (IGF), tumour growth factor-α (TGF-α), tumour growth factor-β (TGF-β), acidic fibroblast growth factor (aFGF), dan basic fibroblast growth factor (bFGF).[1,2]
Direvisi oleh: dr. Dizi Bellari Putri