Penatalaksanaan Wilms Tumor (Nefroblastoma)
Penatalaksanaan Wilms tumor, atau nefroblastoma, dapat berupa tindakan bedah saja, atau diikuti dengan kemoterapi, radioterapi, dan re-operasi intensif. Faktor yang berkaitan dengan pemilihan terapi adalah kondisi tumor unilateral atau bilateral, stadium tumor lokal, ada tidaknya metastasis, usia pasien, ukuran tumor, faktor risiko biologis, histologi, dan respon terhadap terapi.[3,4]
Pembedahan
Tindakan bedah direkomendasikan pada seluruh pasien anak dengan Wilms tumor unilateral pada saat tegak diagnosis. Meskipun penentuan stadium dilakukan sebelum operasi dengan modalitas pencitraan CT scan atau MRI, namun tindakan bedah untuk mengeksplorasi massa tumor secara langsung harus dilakukan. Jaringan yang diangkat digunakan untuk evaluasi patologi.[3]
Persiapan dan Tujuan Pembedahan
Sebelum tindakan operasi, penting untuk menentukan apakah tumor dapat direseksi, jenis dan waktu yang tepat untuk operasi, dan apakah diperlukan kemoterapi neoadjuvan untuk mengecilkan ukuran tumor sebelum operasi. Evaluasi resektabilitas tumor meliputi jumlah dan perluasan tumor, risiko gangguan paru akibat metastasis, risiko morbiditas, mortalitas, tumor residu, atau gagal ginjal jangka panjang.
Tujuan utama dari tindakan bedah yaitu menentukan ukuran dan perluasan dari massa tumor, mengevaluasi adenopati retroperitoneal, ruptur tumor, serta asites, juga mengevaluasi keterlibatan vena renalis atau vena cava inferior. Pengangkatan seluruh tumor harus dilakukan tanpa adanya ruptur atau ceceran tumor, disertai evaluasi stadium nodus limfa, dan evaluasi patologi lengkap.[3]
Metode Operasi
Metode operasi yang lebih disukai yaitu transabdominal atau torakoabdominal dengan pendekatan transperitoneal untuk menghindari tumpahan tumor. Tindakan bedah yang dilakukan meliputi penilaian ukuran dan perluasan tumor, eksplorasi abdomen, serta pengambilan sampel nodus limfatik dengan minimal 5 nodus dari hilus renalis yang terhubung dengan ginjal, parakaval, dan para-aortik.
Terjadinya tumpahan tumor pada saat tindakan operasi harus didokumentasikan. Pasien dengan tumpahan tumor diklasifikasikan sebagai stadium III dan harus menerima radioterapi. Pada kasus tumor bilateral dengan predisposisi genetik atau risiko tinggi gagal ginjal, perlu dilakukan nephron-sparing surgery (NSS). Di sisi lain, NSS tidak direkomendasikan pada tumor unilateral atau tanpa predisposisi genetik.[3]
Kemoterapi
Kemoterapi pada kasus Wilms tumor direkomendasikan sebagai kombinasi dengan tindakan bedah dan radioterapi. Pemberian kemoterapi telah dikaitkan dengan peningkatan kesintasan. Meski begitu, evaluasi mengenai rasio manfaat dan risikonya harus dilakukan dengan cermat.
Regimen kemoterapi dapat mencakup kombinasi vincristine dan dactinomycin. Alternatif lain adalah kombinasi vincristine, dactinomycin, dan doxorubicin.[3,4]
Tabel 1. Pilihan Regimen Kemoterapi pada Wilms Tumor
| Regimen | Nama dan Dosis Obat |
| EE4A | Vincristine 13 dosis |
| Dactinomycin 7 dosis | |
| Regimen diberikan selama 18 minggu. | |
| DD4A | Vincristine 15 dosis (10 dosis diberikan setiap minggu, 5 dosis diberikan setiap 3 minggu) |
| Dactinomycin 5 dosis | |
| Doxorubicin 4 dosis (dosis kumulatif 150 mg/m2) | |
| Regimen diberikan selama 24 minggu, dengan dosis alternatif dactinomycin dan doxorubicin setiap 3 minggu. | |
| VAD | Vincristine 12 dosis |
| Dactinomycin 2-4 dosis | |
| Doxorubicin 2-4 dosis (dosis kumulatif 70-140 mg/m2) | |
| Regimen diberikan selama 6-12 minggu berdasarkan respon pengobatan dan jadwal operasi. Regimen ini hanya diberikan pada penggunaan neoadjuvan untuk pasien dengan rencana NSS (nephron-sparing surgery). Pada regimen ini dactinomycin dan doxorubicin diberikan bersamaan. | |
| Regimen M | Vincristine 9 dosis |
| Dactinomycin 5 dosis | |
| Doxorubicin 5 dosis (dosis kumulatif 150 mg/m2) | |
| Cycloposphamide 4 kali 5 dosis harian selama 24 minggu | |
| Etoposide 4 kali 5 dosis harian selama 24 minggu | |
| Regimen diberikan selama 24 minggu. Pada regimen ini dactinomycin dan doxorubicin diberikan bersamaan, serta cyclophosphamide dan etoposide diberikan bersamaan. | |
| Regimen ini diberikan pada minggu ke-7 pada tumor yang memerlukan tambahan terapi berdasarkan penanda molekuler atau respon terhadap metastasis paru pada minggu ke-6 regimen DD4A. |
Sumber: dr. Siti Solichatul Makkiyyah, Alomedika, 2024.[3]
Adanya penanda molekular spesifik, seperti LOH 1p dan 16q, 11p15, serta 1q, yang teridentifikasi pada jaringan tumor berhubungan dengan peningkatan risiko relaps setelah terapi awal. Pemeriksaan sitogenetik dan molekuler untuk 1q ata LOH untuk 1p dan 16q direkomendasikan untuk seluruh anak dengan diagnosis baru Wilms tumor yang favorable
Kemoterapi Neoadjuvan
Regimen kemoterapi neoadjuvan digunakan untuk pasien dengan kontraindikasi atau ketidakmampuan untuk menjalani nefrektomi awal. Kemoterapi ini mencakup regimen EE4A, DD4A, atau VAD. Kemoterapi neoadjuvan direkomendasikan untuk mengecilkan ukuran tumor sebelum tindakan operasi pada anak dengan tumor bilateral, pasien dengan tumor unilateral yang tidak dapat direseksi, pasien dengan kondisi predisposisi, dan tumor unilateral terlokalisir atau metastasis.
Pada minggu ke-6 kemoterapi neoadjuvan, tumor diperiksa ulang untuk menentukan apakah tumor dapat direseksi. Jika ada, lesi paru dapat digunakan untuk menilai respon kemoterapi neoadjuvan. Lesi paru yang persisten dapat dipertimbangkan untuk dioperasi setelah 6 minggu kemoterapi, hanya jika lesi tersebut dapat dioperasi tanpa adanya morbiditas signifikan.
Jika pasien memiliki respon baik terhadap kemoterapi pada minggu ke-6 maka operasi tidak diperlukan. Jika terjadi kurang dari setengah respon parsial setelah kemoterapi, maka biopsi terbuka diperlukan untuk menilai anaplasia atau untuk mengonfirmasi diagnosis Wilms Tumor. Kemoterapi dilanjutkan selama 12 minggu jika pasien mengalami respon parsial pada minggu ke-6, termasuk NSS.[3]
Kemoterapi Adjuvan
Kemoterapi adjuvan diberikan dalam kurun waktu 7-14 hari setelah tindakan operasi dengan regimen meliputi EE4A, DD4A, dan regimen M. Pemberian regimen didasarkan pada stratifikasi risiko dan kondisi masing-masing pasien.[3]
Radioterapi
Radioterapi (RT) adjuvan direkomendasikan untuk pasien dengan risiko lebih tinggi setelah operasi dan tidak untuk pasien dengan penyakit stadium rendah dan risiko lebih rendah. RT flank adjuvan dengan atau tanpa iradiasi seluruh paru dapat direkomendasikan. NCCN merekomendasikan agar RT dimulai idealnya pada hari ke-10 pascaoperasi, dan tidak lebih dari hari ke-14.
Radiasi flank diindikasikan pada pasien dengan stadium lokal III atau IV dengan stadium local III. Radiasi whole abdomen (WAI) direkomendasikan untuk pasien dengan asites positif sitologi, ruptur tumor pra operasi, perluasan ke peritoneum, dan tumpahan bedah difus.[3]
Perhatian Khusus Terkait Radioterapi
Pelindung testis direkomendasikan untuk sebagian besar anak laki-laki yang menerima radioterapi. Jika RT dipertimbangkan, jadwal harus dikoordinasikan dengan kemoterapi untuk menghindari pemberian dosis penuh dactinomycin atau doxorubicin bersamaan dengan RT.
Adjuvan iradiasi seluruh paru direkomendasikan untuk pasien dengan metastasis paru. IMRT (intensity-modulated RT) atau AP/PA (anteroposterior/posteroanterior) dapat digunakan. Faktor pasien harus dipertimbangkan saat memutuskan jadwal RT adjuvan, termasuk usia dan kebutuhan untuk menilai respons metastasis paru terhadap kemoterapi saat memberikan WAI dan iradiasi seluruh paru.[3]
Stratifikasi Risiko
Stratifikasi risiko dapat digunakan untuk menentukan strategi penatalaksanaan terbaik pada Wilms tumor. Risiko diukur dengan mengevaluasi tampilan histopatologi, stadium tumor, penanda molekuler, adanya metastasis, penyakit bilateral, serta faktor klinis yang meliputi usia anak, ada tidaknya sindroma predisposisi, dan respon lesi paru terhadap kemoterapi neoadjuvan.[3]
Tabel 2. Penilaian Status Risiko Wilms Tumor
| Usia | Berat Tumor | Stadium | Kelompok Risiko Awal | LOH 1p/16q | Respon Metastasis Paru | Metastasis Ekstra-Paru | Kelompok Risiko Akhir |
| <2 tahun | <550 g | I | Sangat rendah | Apapun | - | - | Sangat rendah |
| Berapapun | >550 g | I | Rendah | Tidak | - | - | Rendah |
| >2 tahun | Berapapun | I | Rendah | Tidak | - | - | Rendah |
| Berapapun | Berapapun | II | Rendah | Tidak | - | - | Rendah |
| BerapapunI | >550 g | I | Rendah | Ya | - | - | Standar |
| >2 tahun | Berapapun | I | Rendah | Ya | - | - | Standar |
| BeIIIrapapun | Berapapun | II | Rendah | Ya | - | - | Standar |
| Berapapun | Berapapun | III | Standar | Tidak | - | - | Standar |
| Berapapun | Berapapun | IV | Lebih Tinggi | Tidak | Lengkap | Tidak | Standar |
| Berapapun | Berapapun | III | Standar | Ya | - | - | Lebih Tinggi |
| Berapapun | Berapapun | IV | Lebih Tinggi | Ya | Apapun | Apapun | Lebih Tinggi |
| Berapapun | Berapapun | IV | Lebih Tinggi | Apapun | Parsial | Apapun | Lebih Tinggi |
| Berapapun | Berapapun | IV | Lebih Tinggi | Apapun | Apapun | Ya | Lebih Tinggi |
| Berapapun | Berapapun | V | Bilateral | Apapun | Apapun | Apapun | Bilateral |
Sumber: dr. Siti Solichatul Makkiyyah, Alomedika, 2024.[2-4]
Klasifikasi berdasarkan kelompok risiko bertujuan untuk menilai terapi yang paling tepat untuk pasien sesuai dengan beberapa kondisi pada pasien, dengan tujuan akhir untuk memaksimalkan luaran terapi dan meminimalkan risiko toksisitas terapi.[3]
Penatalaksanaan Wilms Tumor Berdasarkan Skenario Klinis
Pilihan penatalaksanaan Wilms tumor yang lebih spesifik dapat ditentukan berdasarkan kondisi tumor. Pada pasien yang menjalani nefrektomi radikal, seluruh bagian ginjal diangkat namun kelenjar adrenal tidak perlu diangkat jika tidak ada tumor yang terlibat. Sementara itu, pada tumor bilateral, tata laksana yang dianjurkan berupa kemoterapi neoadjuvan dengan regimen VAD diikuti dengan operasi NSS (nephron-sparing surgery) untuk mempertahankan fungsi ginjal.
Kriteria klinis yang memungkinkan untuk dilakukan tindakan NSS yaitu ukuran tumor kecil, lokasi massa perifer atau polar, serta minimnya keterlibatan atau invasi pada pembuluh darah renal. Sementara itu, kontraindikasi relatif dari NSS adalah lokasi sentral dan lokasi yang sangat dekat dengan pembuluh darah ginjal.
Jika memungkinkan, dapat dilakukan NSS bilateral. Pada kasus dengan respon parsial terhadap kemoterapi, pertimbangkan biopsi terbuka untuk menilai ada tidaknya anaplasia. Lanjutkan kemoterapi jika pasien belum dapat menjalani NSS. Operasi harus dilakukan dalam 12 minggu dari dimulainya terapi neoadjuvan. Jika terjadi kekambuhan, NSS dapat diulang.[3]
Algoritma Tata Laksana Wilms Tumor Unilateral
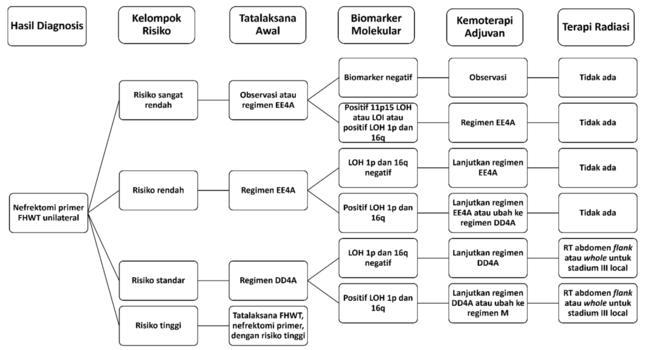
Pada kasus Wilms tumor unilateral, terapi dipilih berdasarkan tingkat risiko pasien. Pada kasus Wilms tumor unilateral, tata laksana standar berupa nefrektomi primer diikuti dengan terapi adjuvan. Namun, pada pasien dengan risiko sangat rendah, pemberian terapi adjuvan pasca nefrektomi dapat dihilangkan. Kriteria pasien dengan risiko rendah ini yaitu usia kurang dari 2 tahun, berat tumor kurang dari 550 gram, dan stadium penyakit I.
Pasca nefrektomi, pemeriksaan biomarker molekular tetap dilakukan untuk memastikan apakah pasien berisiko lebih tinggi terhadap kekambuhan. Pasien dengan kriteria risiko sangat rendah namun dengan penanda molekular unfavorable, yaitu positif terhadap LOH atau LOI 1p15 atau LOH 1p dan 16q, akan memerlukan kemoterapi adjuvan dengan regimen EE4A. Radioterapi tidak direkomendasikan untuk pasien stadium I.[3]
Gambar 1. Algoritma Tata Laksana Wilms Tumor Unilateral.[3]
Pasien dengan hasil penilaian risiko standar direkomendasikan untuk diberikan terapi DD4A. Pada minggu ke-6 kemoterapi, hasil pemeriksaan molekular digunakan untuk menentukan penilaian risiko akhir dan pemberian terapi selanjutnya. Pada pasien dengan hasil molekular positif terhadap LOH 1p dan 16q, direkomendasikan untuk berganti ke regimen M.
RT flank atau WAI direkomendasikan pada pasien dengan tumor lokal stadium III. Jika RT diberikan pada pasien, diperlukan koordinasi untuk mencegah pemberian bersamaan antara dactinomycin dan doxorubicin dosis penuh dengan RT.[3]
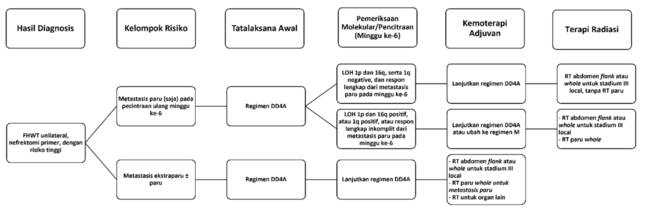
Gambar 2. Algoritma Tata Laksana Wilms Tumor Risiko Tinggi.[3]
Pasien dengan Wilms tumor stadium IV diklasifikasikan sebagai risiko tinggi dan direkomendasikan menjalani terapi dengan DD4A. Pada minggu ke-6, hasil pemeriksaan molekular digunakan untuk menentukan penilaian risiko akhir dan pemberian terapi selanjutnya. Pada pasien dengan hasil molekular positif terhadap LOH 1p dan 16q atau respon lambat inkomplit terhadap metastasis paru, direkomendasikan untuk berganti ke regimen M.
Sementara itu, pasien dengan respon lengkap pada metastasis paru dan ekstra-paru dapat melanjutkan pemberian terapi DD4A. RT whole lung direkomendasikan pada semua pasien dengan metastasis paru, kecuali pasien dengan respon komplit terhadap kemoterapi pada minggu ke-6, dan negatif terhadap LOH 1p dan 16q, 1q gain, atau metastasis ekstra-paru lain.[3]
Algoritma Tata Laksana Wilms Tumor Unilateral Unresectable Tanpa Predisposisi
Pasien dengan tumor ginjal unilateral yang tidak dapat direseksi dini dan tanpa kondisi predisposisi direkomendasikan untuk mendapatkan terapi neoadjuvan dengan DD4A. Biopsi direkomendasikan pada seluruh pasien dengan kriteria untuk reseksi tertunda, dengan tujuan untuk menentukan histologi, penegakan diagnosis Wilms tumor, dan menguji marker molekular.
Pada minggu ke-6, dilakukan pencitraan ulang untuk menentukan apakah pasien dapat menjalani nefrektomi dan sampling nodus limfa regional atau harus tetap melanjutkan terapi DD4A hingga minggu ke-12. Selanjutnya, operasi direkomendasikan pada seluruh pasien pada maksimal minggu ke-12 dari kemoterapi neoadjuvant.
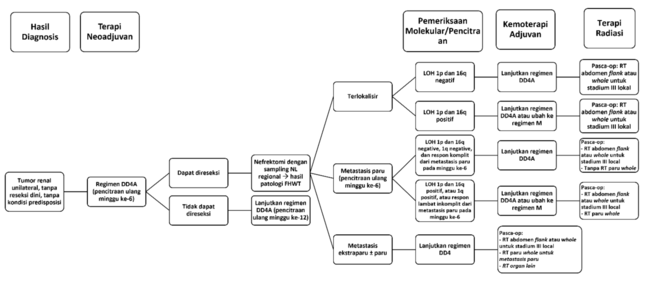
Jika pemeriksaan patologi telah mengonfirmasi Wilms tumor favorable, hasil pemeriksaan molekular dan pencitraan digunakan untuk menentukan risiko akhir dan terapi lanjutan. Perubahan terapi menjadi regimen M direkomendasikan pada pasien dengan peningkatan risiko.[3]
Gambar 3. Algoritma Tata Laksana Wilms Tumor Unilateral Unresectable Tanpa Predisposisi.[3]
Algoritma Tata laksana Wilms Tumor Unilateral Terlokalisir dengan Predisposisi
Pasien dengan tumor unilateral terlokalisir dengan kondisi predisposisi direkomendasikan untuk mendapat terapi neoadjuvan dengan regimen EE4A. Biopsi maupun reseksi sangat dihindari pada kondisi ini. Namun, jika biopsi dilakukan, maka regimen VAD digunakan sebagai terapi neoadjuvan.
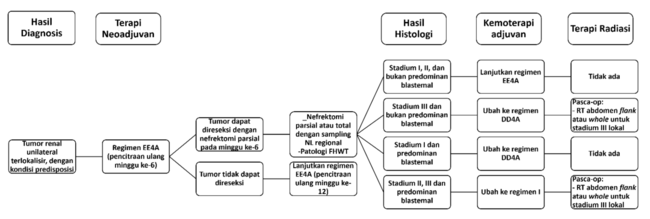
Pada minggu ke-6, dilakukan pencitraan ulang dan evaluasi terhadap respon kemoterapi neoadjuvan. Pasien tidak perlu operasi jika respon komplit terhadap EE4A atau VAD. Pasien dianjurkan menjalani nefrektomi parsial dengan sampling nodus limfa jika tumor dapat direseksi. Regimen EE4A atau VAD dilanjutkan maksimal hingga 12 minggu jika tumor masih tidak dapat direseksi namun menunjukkan setidaknya respon parsial. Nefrektomi total dianjurkan pada pasien dengan setidaknya respon parsial.[3]
Gambar 4. Algoritma Tata Laksana Wilms Tumor Unilateral Terlokalisir dengan Predisposisi.[3]
Penentuan regimen kemoterapi didasarkan pada penilaian risiko akhir. Pasien dengan respon komplit terhadap regimen EE4A pada minggu ke-6 dapat melanjutkan regimen EE4A tanpa perlu RT. Sementara itu, pergantian ke regimen DD4A direkomendasikan pada pasien dengan peningkatan risiko.[3]
Algoritma Tata laksana Wilms Tumor Unilateral Metastasis dengan Predisposisi
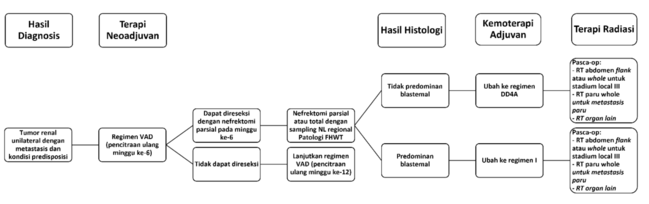
Pada pasien dengan Wilms tumor unilateral bermetastasis dan dengan kondisi predisposisi, direkomendasikan pemberian kemoterapi neoadjuvan dengan regimen VAD. Pada minggu ke-6, dilakukan pencitraan ulang dan pasien tidak perlu tindakan operasi jika terjadi respon lengkap terhadap regimen VAD. Nefrektomi parsial dilakukan jika tumor dapat direseksi. Sementara itu, VAD dilanjutkan hingga 12 minggu jika tumor belum dapat direseksi namun menunjukkan setidaknya respon parsial.[3]
Gambar 5. Algoritma Tata Laksana Wilms Tumor Unilateral Metastasis dengan Predisposisi.[3]
Jika pada minggu ke-6 respon parsial tidak tercapai, harus dilakukan biopsi untuk mengonfirmasi diagnosis sebelum melanjutkan terapi regimen VAD. Tindakan operasi nefrektomi total atau parsial direkomendasikan untuk dilakukan pada minggu ke-12 setelah pemberian kemoterapi neoadjuvan dimulai. Keputusan nefrektomi total atau parsial didasarkan pada ukuran, lokasi, dan perluasan tumor, serta faktor lainnya.[3]
Algoritma Tata laksana Wilms Tumor Bilateral
Pasien dengan WT bilateral memiliki insidensi sindroma predisposisi yang lebih besar dan lebih berisiko untuk mengalami tumor metakronos setelah terapi. Pasien dengan tumor bilateral memiliki kesintasan yang lebih rendah karena understaging dan peningkatan risiko histologi anaplastik. Tujuan terapi pada Wilms tumor bilateral adalah meningkatkan kesintasan dan mempertahankan fungsi ginjal sebaik mungkin.[3]
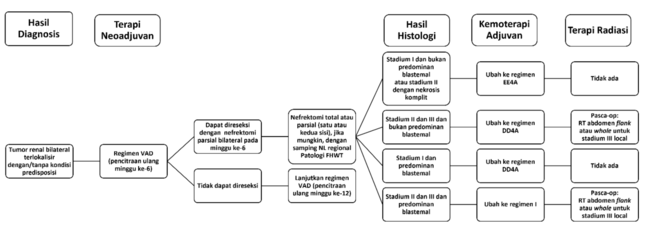
Gambar 6. Algoritma Tata Laksana Wilms Tumor Bilateral Terlokalisir dengan atau Tanpa Predisposisi.[3]
Pasien dengan tumor bilateral terlokalisir dengan atau tanpa kondisi predisposisi direkomendasikan untuk mendapat kemoterapi neoadjuvan dengan regimen VAD. Biopsi atau reseksi dini tidak disarankan pada kondisi ini. Operasi dilakukan pada minggu ke-6 atau 12 setelah kemoterapi neoadjuvan dilakukan. Operasi yang direkomendasikan adalah NSS (Nephron-sparing surgery).[3]
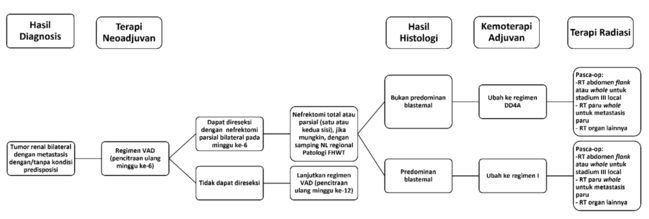
Gambar 7. Algoritma Tata Laksana Wilms Tumor Bilateral Metastasis dengan atau Tanpa Predisposisi.[3]
Pasien dengan tumor bilateral bermetastasis dengan atau tanpa kondisi predisposisi direkomendasikan untuk mendapat kemoterapi neoadjuvan dengan regimen VAD. Biopsi atau reseksi dini tidak disarankan pada kondisi ini. Pada minggu ke-6 kemoterapi, dilakukan pencitraan ulang dan pasien tidak perlu operasi jika memiliki respon komplit terhadap VAD. Di sisi lain, jika tumor dapat direseksi, maka dilakukan nefrektomi parsial bilateral. Jika tumor tetap tidak dapat direseksi, maka lanjutkan regimen VAD hingga minggu ke-12.
Jika terdapat respon kurang dari parsial pada minggu ke-6, direkomendasikan biopsi ginjal pada kedua ginjal untuk menentukan histologi sebelum melanjutkan VAD. Operasi dilakukan pada minggu ke-6 atau 12 setelah kemoterapi neoadjuvan dilakukan. Operasi yang direkomendasikan adalah NSS (Nephron-sparing surgery).[3]
Follow-up
Tindak lanjut pasca penanganan Wilms tumor meliputi surveilans dengan pemeriksaan pencitraan pada toraks dan abdomen setiap 3 bulan selama 2 tahun. Ini kemudian dilanjutkan dengan pemeriksaan setiap 6 bulan selama 2 tahun, baru kemudian sekali setiap dua tahun. Modalitas yang dapat digunakan yaitu rontgen toraks dan USG abdomen.[1]
Penulisan pertama oleh: dr. Apri Haryono Hafid